Infecção latente de tuberculose (ILTB) em PVHA
Estima-se que um 1/3 da população mundial esteja infectado pelo M. tuberculosis. A maior parte da população infectada não adoece e desenvolve imunidade parcial à doença.
Já entre as pessoas vivendo com HIV/aids (PVHA) que estão concomitantemente infectadas pelo Mycobacterium tuberculosis (ou seja, com tuberculose latente), estima-se que 10% desenvolvam a tuberculose ativa a cada ano.
Diferença entre ILTB e tuberculose ativa
Para uma melhor compreensão do tema tuberculose latente ou infecção latente da tuberculose, é importante recordar que o bacilo da tuberculose, após infectar um organismo, pode permanecer latente, sem causar doença, por muitas décadas. Ou seja, a infecção latente de tuberculose (ILTB) é um estado em que o indivíduo tem o Mycobacterium tuberculosis, mas não tem nenhum sintoma ou manifestação da doença.
A exposição ao bacilo da tuberculose ocorre a partir de um doente que tosse e expele bacilos. Somente 30% dos expostos se infectam. Na população geral, dentre os infectados, 5% a 10% desenvolvem a tuberculose doença nos primeiros dois anos após a infecção. A maioria (de 90% a 95%) das pessoas permanece com a infecção na forma latente. Tardiamente (após os primeiros anos), outros 5% reativam o foco latente em algum momento, pelos mais variados motivos (diabetes, uso de imunossupressores, etc.).
Entre as PVHA, 5% a 15% dos que têm a ILTB reativam o foco latente de tuberculose a cada ano.
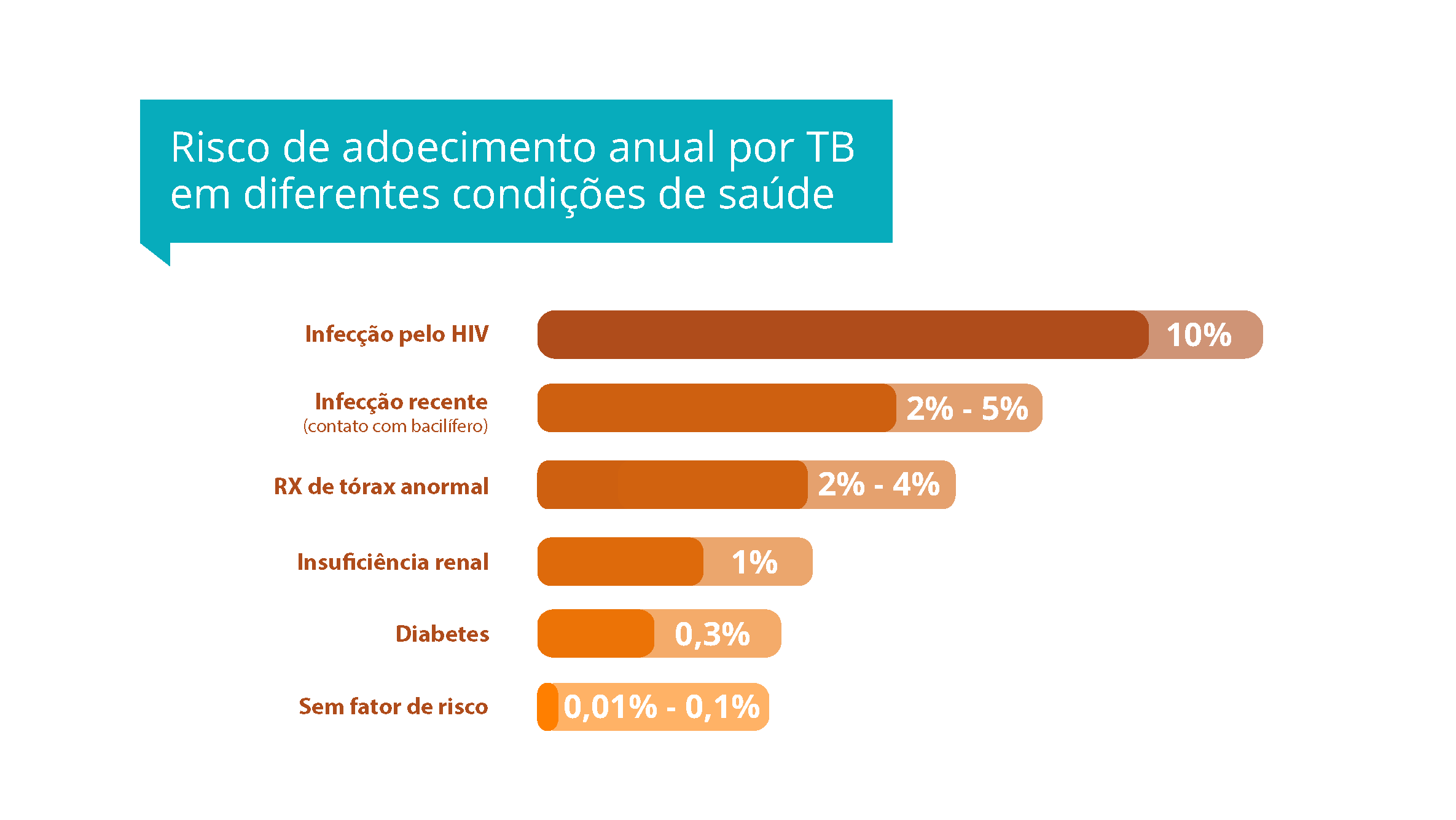
Dentre todas as possíveis causas de reativação de focos latentes de tuberculose, como diabetes, desnutrição e insuficiência renal, a infecção pelo HIV é o maior fator de risco para o desenvolvimento de tuberculose ativa.
Veja abaixo o risco de adoecimento por tuberculose frente a diferentes condições de saúde. Note que a infecção pelo HIV é o principal fator de risco para o desenvolvimento de tuberculose.
Diagnóstico da ILTB
Para evitar que a infecção latente se converta em tuberculose ativa (doença), é necessário diagnosticar a tuberculose latente e instituir o tratamento da ILTB.
No Brasil, o diagnóstico da TB latente (ILTB) se faz pelo exame clínico, perguntas e também pela prova tuberculínica (PT), exame realizado pela inoculação intradérmica de PPD (derivado proteico purificado), com posterior leitura do tamanho da enduração (após 72 horas da aplicação).
A prova tuberculínica não é um bom exame para o diagnóstico da tuberculose ativa, mas é um bom teste para o diagnóstico da infecção latente. Nas pessoas vivendo com o HIV, esse é um exame fundamental para evitar o adoecimento pela tuberculose.
Em PVHA, recomenda-se que a PT seja feita anualmente, caso o último resultado tenha sido negativo.
A PT é considerada negativa quando a leitura é menor do que 5 mm e é considerada positiva quando for maior ou igual a 5mm. Frente a um resultado positivo, deve-se afastar a possibilidade de tuberculose ativa (por meio da anamnese clínica e, quando possível, da radiografia de tórax) e tratar a ILTB.
É importante lembrar que em PVHA que estejam com a contagem de linfócitos T-CD4+ menor do que 200 cél/mm3, a PT será negativa (anérgica) e, portanto, não tem utilidade. Nesses casos, deve-se aguardar a reconstituição imune para repetir a PT.
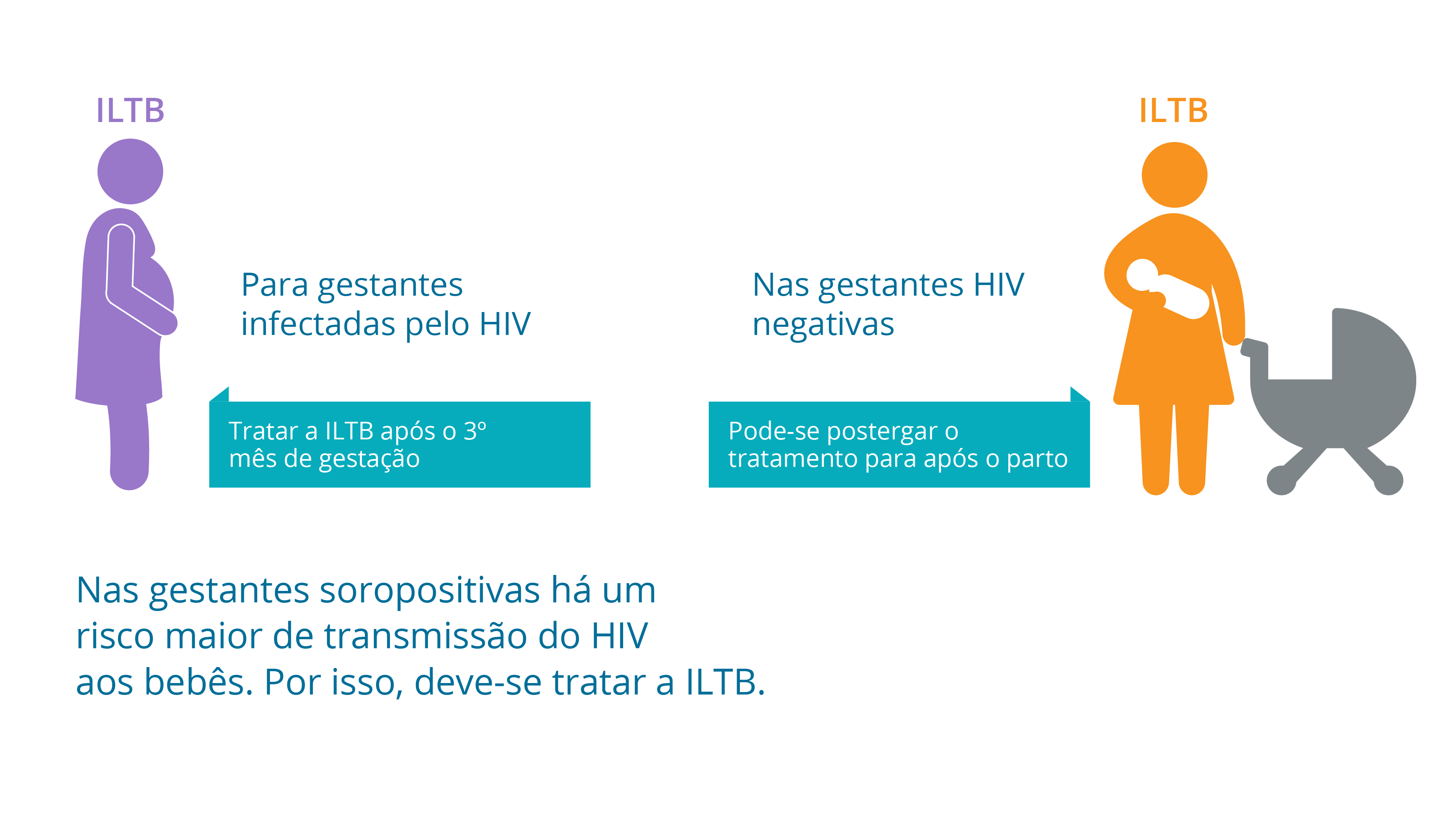
Outro aspecto importante é que a infecção latente da tuberculose tem especial relevância em gestantes infectadas pelo HIV. É muito importante prevenir que as gestantes vivendo com HIV/aids tenham tuberculose ativa porque quando isso acontece, há aumento de sua carga viral com consequente aumento do risco de transmitir o HIV para seus bebês. Assim, nesse grupo, recomenda-se tratar a infecção latente após o 3º mês de gestação.
Indicações de tratamento da ILTB
O tratamento da infecção latente vai ser recomendado nas seguintes situações:
- PVHA com radiografia de tórax normal e:
- prova tuberculínica ≥ a 5 mm; ou
- que tenha tido contato com um caso de tuberculose pulmonar, independentemente do resultado da prova tuberculínica; ou
- que tenha registro documental de ter tido PT ≥ 5 mm e não ter se submetido ao tratamento da ILTB na ocasião.
- PVHA com cicatriz radiológica sem tratamento prévio da infecção latente da tuberculose, independentemente do resultado da prova tuberculínica.
Considerando um recente desabastecimento temporário de PPD no Brasil para a realização da Prova Tuberculínica, é importante conhecer a Nota Informativa nº 8, de 2014, CGPNCT/DEVEP/SVS/MS, que dispõe sobre algumas especificidades de indicações do tratamento da ILTB em PVHA nessas situações.
Tratamento da ILTB
O fármaco usado no tratamento da ILTB é a isoniazida. No Brasil, este medicamento está disponível somente na rede pública em comprimidos de 100 mg. A dose recomendada é de 5 mg/kg a 10 mg/kg de peso até a dose máxima de 300 mg/dia. Dessa forma, de acordo com as faixas de peso, as recomendações são as seguintes:
- 20 kg a 35 kg – 2 comprimidos de 100 mg/dia;
- 36 kg e 50 kg – 2 a 3 comprimidos/dia; e
- Acima de 50 kg – 3 comprimidos/dia.
O tratamento da ILTB em PVHA deve ser realizado, idealmente, com 270 doses, por um período mínimo de nove meses, que pode ser estendido para 12 meses.
Há evidências de que o uso da isoniazida por nove meses protege mais do que o uso por seis meses, principalmente em pacientes com HIV/aids. Para fazer a opção entre seis meses (com 180 doses) e nove meses (com 270 doses) de tratamento deve-se considerar a viabilidade operacional e a adesão do paciente.
A quantidade de doses tomadas é mais importante do que o tempo de tratamento. Por isso, recomenda-se que esforços sejam feitos para que o paciente complete o total de doses programadas mesmo com a eventualidade de uso irregular, considerando a possível prorrogação do tempo de tratamento com o objetivo de completar as doses previstas, não excedendo esta prorrogação em até três meses do tempo inicialmente programado.
Em gestantes, durante o tratamento da ILTB com a isoniazida, recomenda-se o uso de piridoxina na dose de 50 mg/dia, diariamente, para reduzir o risco de toxicidade neurológica no recém-nascido.
Referências
AMERICAN THORACIC SOCIETY. Targeted tuberculin testing and treatment of latent tuberculosis infection. American Journal of Respiratory and Critical Care Medicine, New York, v. 161, p. S221-S247, 2000.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Guia de Vigilância em Saúde. Brasília: Ministério da Saúde, 2014.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância Epidemiológica. Manual de recomendações para o controle da tuberculose no Brasil. Brasília: Ministério da Saúde, 2011.
BRASIL. Ministério da Saúde. Secretaria-Executiva. Recomendações para o manejo da coinfecção TB-HIV em serviços de atenção especializada a pessoas vivendo com HIV/AIDS. Brasília: Ministério da Saúde, 2013.
COMSTOCK, G. W. How much isoniazid is needed for prevention of tuberculosis among immunocompetent adults? International Journal of Tuberculosis and Lung Disease, Paris, v. 3, n. 10, p. 847-850, 1999.
FARGA, V.; CAMINERO J. A. Tuberculosis. 3. ed. Santiago, Chile: Editora Mediterraneo, 2011.
FOCCACIA, R. Tratado de Infectologia. 4. ed. São Paulo: Editora Atheneu, 2010.
GUPTA, A. et al. Maternal Tuberculosis: A Risk Factor for Mother-to-Child Transmission of Human Immunodeficiency Virus. The Journal of Infectious Diseases, v. 203, 1st Feb 2011, p. 358-363.
MANDELL, G. L.; BENNET J. E.; DOLIN, R. Mandell, Douglas and Bennett's Principles and Practice of Infectious Diseases. Elsevier: 7th ed, 2010.